
El cannabis está cada vez más disponible para el uso médico y recreativo, por lo que constituye hoy en día un tema de obligatoria revisión para el personal de salud y los pacientes que tienen patologías relacionadas con el dolor crónico, epilepsia y trastornos psiquiátricos.
Sistema endocannabinoide.
El sistema endocannabinoide consiste en una red de comunicación intercelular en varios tejidos del cuerpo, cuyo objetivo es regular varios procesos fisiológicos del organismo. Se compone de receptores que son proteínas de membrana celular y los endocannabinoides propiamente dichos que son lípidos que llevan una señal molecular y se unen a los receptores.
Normalmente en la sinapsis, que es la unión de dos neuronas, hay una neurona presináptica, que libera un neurotransmisor y la neurona postsináptica que capta ese neurotransmisor para ejercer una función fisiológica.
En el caso de los endocannabinoides tienen la particularidad de actuar en forma retrograda, hacen lo contrario, son secretados por la neurona postsináptica a al espacio sináptico, y son las células presinápticas que tienen el receptor y el efecto fisiológico es regulatorio, limitando la liberación de otros neurotransmisores.

Grafico 1. Representación esquemática del mecanismo de acción de los endocannabinoides: La mayoría de neurotransmisores (NT) producidos en la neurona presináptica (PRE), son almacenados en vesículas (VS) y son liberados al espacio sináptico cuando se produce un potencial de acción (no representado). El NT se une a un receptor en la neurona postsináptica (POST) donde ejerce su actividad fisiológica.
Los endocannabinoides (EC) a diferencia de los NT no son almacenados, sino que se sintetizan en el momento en que se requieren a partir del precursor fosfatidiletanolamina, los EC son liberados al espacio sináptico y se unen al receptor CB1 ejerciendo una retroalimentación negativa impidiendo la formación, almacenamiento y liberación del NT.
Receptores cannabinoides.
Los receptores cannabinoides se dividen en dos:
Receptores cannabinoides CB1.
Están ubicados en grandes cantidades en el cerebro (ganglios basales, cortex, cerebelo e hipocampo), actúan regulando la secreción de otros neurotransmisores tal como el GABA y el Glutamato. También se encuentran en menos cantidad en la médula espinal.
Pero los receptores CB1 no son exclusivos del cerebro, también se encuentran en el sistema gastrointestinal (páncreas, intestino e hígado), sistema vascular, músculo y órganos reproductivos, aunque en mucho menos cantidades.
Receptores cannabinoides CB2.
Aunque los receptores CB2 están también presentes en el cerebro, en donde se cree están encargados de mediar las emociones. Este tipo de receptores se ubican más en la periferia: bazo, huesos, piel páncreas y sistema inmune, son especialmente abundantes en las células sanguíneas de la línea blanca.
Neurotransmisores endocannabinoides.
Los endocannabinoides se derivan del ácido graso omega 6 Ácido Araquidónico (AA) y los más importantes son dos:
Anandamida (Araquidonoiletanolamina).
La anandamida es conocido como el neurotransmisor de la felicidad, en efecto “ananda” en el lenguaje sánscrito traduce felicidad. Es una molécula que produce relajación de casi todos los tejidos, los efectos en el cerebro se manifiestan con sedación.
A diferencia de otros neurotransmisores, no se almacena, se fabrica en el momento en que se necesita y es inactivada a los pocos segundos.
Sus funciones están en el control de otros neurotransmisores contribuyendo a la homeostasis, a la disminución de la percepción del dolor, disminuye la proliferación del cáncer (metástasis), en bajas dosis aumenta la lívido, y tiene efectos en la memoria y en la capacidad de automotivación.

Grafico 2. Estructura química de los endocannabinoides.
2-Araquinodilglicerol (2-AG).
El 2-AG es el endocannabinoide más abundante en el humano, sin embargo, sus funciones todavía no están del todo bien entendidas, en el momento de escribir este artículo, se emplea como posible diana para la fabricación de medicamentos contra la obesidad.
Mecanismo intracelular de los endocannabinoides.
Los mecanismos de acción intracelular todavía no son totalmente entendidos por la ciencia, se cree que los cannabinoides tienen efecto en el decremento del AMPc intracelular, mediado por inhibición de la enzima adenilciclasa, con el consecuente incremento en la vía MAPK/ERK/MEK. Pero es posible que otras vías moleculares estén también implicadas.
Fitocannabinoides
Como estudiamos en el blog de las propiedades nutricionales de la semilla de cáñamo, publicado recientemente, los fitocannabinoides se encuentra en las flores, las hojas, los retoños y el tallo de la planta, y están ausentes en raíz y semillas del cáñamo.
Son más de 70 los fitocannabinoides aislados, pero solo unos pocos han sido estudiados, dentro de ellos el CBD (cannabidiol), el THC (Tetrahidrocannabidiol) y CBG (Cannabigerol), y son los dos primeros los que se emplean en el cannabis medicinal.

Grafico 3. Estructura química de los fitocannabinoides.
El cannabis medicinal tiene su base en los fitocannabinoides, y los efectos de estos compuestos son mucho más amplios que los endocannabinoides, como veremos a continuación:
Unión a los receptores acoplados a proteínas G (GPR)
Activación del receptor serotoninérgico 5HT1A
La activación del receptor de serotonina 5HT1A, explica los efectos ansiolíticos y antidepresivos del CBD (medicamentos como la buspirona y fluoxetina tienen un mecanismo de acción similar).
La activación de este mismo receptor 5HT1A es responsable de reducción del dolor (el sumatriptan es un medicamento empleado para tratamiento de crisis de migraña y emplea este mismo mecanismo).
Los efectos del CBD en el ciclo del sueño y deseo sexual también tienen que ver con la activación del 5HT1A (flibanserin, un medicamento recientemente aprobado por la FDA para mejorar el deseo sexual de mujeres postmenopáusicas, emplea este mecanismo).
Antagonismo de receptores GPR
El antagonismo de los GPR3, GPR6 y GPR 12 se manifiestan en la disminución del dolor y disminución de la actividad proliferativa celular.
Agonismo parcial de receptores Dopamnérgicos D2 (D2, D3, D4)
Agonismo parcial del receptor Dopaminérgico D2 (inhiben la formación de cAMP y activan los canales de K), lo que explicaparte de los efectos antidepresivos y su potencial uso en manejo de trastornos del movimiento (Parkinson).
Receptores Ionotrópicos.
Activación de canales TRP
El CBD activa algunos canales de potencial de receptor transitorio (Transient Potencial Receptor), En este sentido el agonismo del CBD por el TPRA1,TPRV1 y TPRV4 explica en gran medida su efecto analgésico.
Antagonismo de receptores GABAergicos
Otra actividad importante es el agonismo de varios tipos de receptores de GABA (neurotransmisor inhibitorio) lo que explica su uso en tratamiento de epilepsia refractaria.
Unión a transportadores intracelulares de endocannabinoides.
El CBD es capaz de unirse transportadores intracelulares de endocannabinoides, algunos estudios han logrado establecer que la unión del CBD con proteínas intracelulares de unión a ácidos grasos, aumenta la disponibilidad de anandamida libre, aumentando su potencial analgésico.
Unión a enzimas.
Citocromo P450.
Los cannabinoides son metabolizados por el complejo enzimático del citocromo P450; El CBD por la isozima CYP3A4, mientras el THC por la isozima CYP2C9; el CBD se une e inhibe la actividad de varias isozimas CYP1B1, CYP2C19, CYP3A7.
Lipoxigenasas.
Inhibe las enzimas Lipoxigenasas (LOX) y por tanto las producción de citoquinas proinflamatorias, lo que puede ser otra explicación en su efecto analgésico.
Enzimas implicadas en el catabolismo de la serotonina y del hidroxitriptófano.
Además, inhibe enzimas implicadas en el catabolismo de la serotonina y el hidroxitriptófano (aralalquinamina-N- acetil transferasa e indolamina-pirrol 2,3 dioxigenasa), lo que potencia los efectos serotoninérgicos vistos anteriormente.
En los complejos mitocondriales.
Un efecto negativo que se ha encontrado es que el CBD inhibe los complejos mitocondriales I, II y IV, sin embargo, su efecto en humanos no ha sido estudiado.
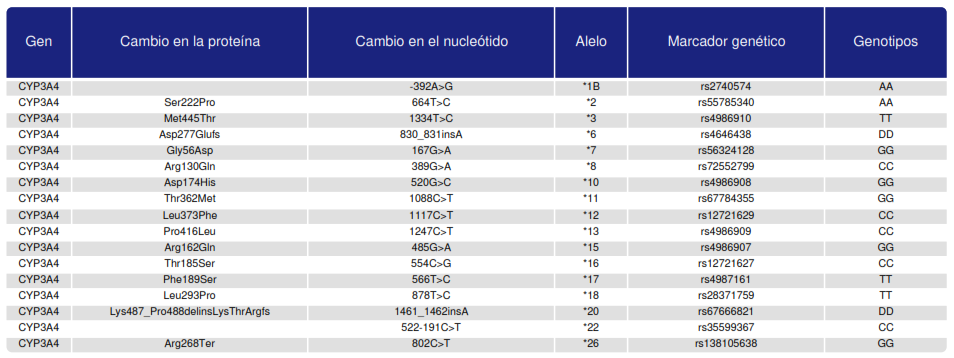
Cuadro 1, 2 y 3. Variables genéticas (SNPs) involucradas en las isozimas CYP2C9, CYP2C19 y CYP3A4 involucrados en el metabolismo del cannabis medicinal y los respectivos medicamentos afectados. Fuente: Reportes de farmacogenética en la práctica médica particular Alimentarte Servicios Médicos.



Unión a factores de transcripción
El CBD es agonista de los factores PPARγ y NRF2 por lo que actúan inhibiendo la transcripción de genes que codifican citoquinas inflamatorias.
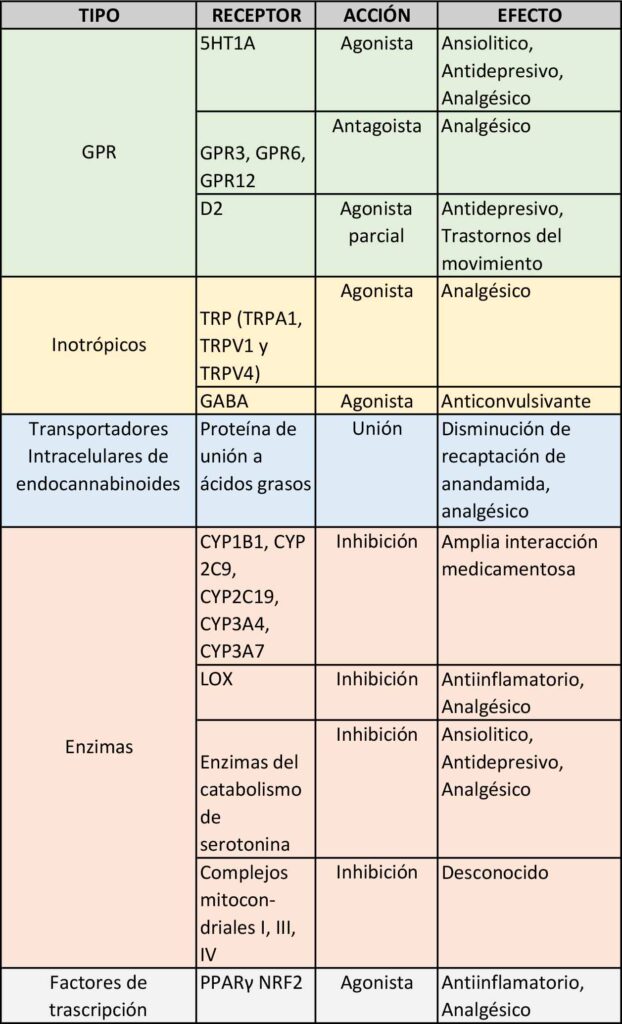
Cuadro 4. Resumen de las interacciones del CBD con diferetes moléculas. Fuente: Elaboración propia.
Fitocannabinoides y dolor.
Como se explicó anteriormente el cannabis medicinal puede tener un papel importante en la regulación de los otros neurotransmisores relacionados con el movimiento, comportamiento, aprendizaje, memoria, reacciones emocionales y principalmente en la percepción del dolor.
Los procedimientos de fabricación de medicamentos en la industria farmacéutica moderna, tienen unos procesos que han sido aprobados por las agencias reguladoras (FDA, EFSA), consisten en extraen los principios activos y se empacan en una presentación (gragea, cápsula suspensión o spray), con el objeto de que los fármacos sean más seguros.
Una paradoja imprevista para la farmacia moderna ha sido que, a pesar del juicioso seguimiento de los procesos antes mencionados, los compuestos aislados no han dado los frutos que se esperaban, y de hecho, moléculas puras o sintéticas aisladas de THC y CBD de grado farmacéutico (nabilona y dronabinol aprobados por la FDA para tratamiento del dolor), no tienen los mismos resultados qué el uso del cannabis medicinal (a esto se le ha llamado efecto séquito).
Esto se podría explicar, debido a qué, existe una sinergia todavía no bien comprendida por la ciencia, entre los diferentes tipos de cannabinoides.
Por esta razón resulta un tanto arbitrario la clasificación actual en que el CBD se cataloga medicinal y el THC recreativo, cuando la realidad es que los diferentes tipos de cannabinoides ejercen una actividad sinérgica que separadamente no son capaces de efectuar por sí solos.
Incluso, un estudio publicado en la prestigiosa revista British Journal of Pharmacology, demostró que la interacción de los fitocannabinoides con otros compuestos bioactivos, los terpenoides, ejercen una sinergia en el manejo del dolor.
CBD homeopatizado, otra de las características de los fitocannabinoides es que su acción se produce en concentraciones de nanomoles.
El cannabis medicinal se puede suministrar sublingual, oral, inhalado y también se absorbe a través de piel.
Las dosis varían pues el metabolismo del CBD que se lleva a cabo en el hígado varía enormemente entre una persona y otra.
Los fitocannabinoides pese a ser compuestos naturales, tienen una amplia interacción con varios medicamentos, como se mostró en los cuadros anteriores.
De cualquier modo, y ateniéndonos a lo que legalmente es posible en la actualidad, los dolores en los que mejor funciona el cannabis medicinal son las polineuropatías (postherpética, diabética, lesión de médula espinal, dolor neuropático por esclerosis múltiple, síndromes de compresión radicular, síndrome del trigémino).
Para efectos prácticos en mis cuatro años de experiencia con el cannabis medicinal, el consejo es empezar de a poco e ir despacio, y utilizar combinación con otros analgésicos o antinflamatorios alopáticos o de origen natural que potencien su efecto analgésico, sin incrementar los efectos adversos.
Como conclusión podemos afirmar que el Cannabis Medicinal (CBD y THC) es una herramienta poderosa para control del dolor crónico, principalmente dolor neuropático, que pese a ser natural interacciona con muchos medicamentos, por lo que se debe hacer una juiciosa historia clínica al formularlo y se debe emplear preferiblemente acompañado de otros analgésicos o antiinflamatorios individualizando el paciente.
Bibliografía
Goodman & Gilman. Las bases farmacológicas de la Terapéutica”. Decimatercera Edición. McGraw Hill
Lucas, C. J., Galettis, P., & Schneider, J. (2018). The pharmacokinetics and the pharmacodynamics of cannabinoids. British journal of clinical pharmacology, 84(11), 2477–2482. https://doi.org/10.1111/bcp.13710
Mlost, J., Bryk, M., & Starowicz, K. (2020). Cannabidiol for Pain Treatment: Focus on Pharmacology and Mechanism of Action. International journal of molecular sciences, 21(22), 8870. https://doi.org/10.3390/ijms21228870
Romero-Sandoval EA, Fincham JE, Kolano AL, Sharpe BN, Alvarado-Vázquez PA. Cannabis for Chronic Pain: Challenges and Considerations. Pharmacotherapy. 2018 Jun;38(6):651-662. doi: 10.1002/phar.2115. Epub 2018 May 16. PMID: 29637590.
https://www.fundacion-canna.es/sistema-endocannabinoide
https://psicologiaymente.com/neurociencias/anandamida
https://bpspubs.onlinelibrary.wiley.com/doi/full/10.1111/j.1476-5381.2011.01238.x








