La Era de las Vacunas RNAm y la Edición Genética, un cambio revolucionario en la Humanidad.

En noviembre de 2018 en una conferencia internacional, el científico chino He JianKui conmocionó al mundo, al anunciar el primer experimento de modificación genética en dos bebés gemelas, cuyo propósito era hacerlas más resistentes al virus de la inmunodeficiencia humana (VIH).
El estupor en la comunidad científica, y la condena en todas las esferas de la ciencia fue unánime, China inició una investigación que llevó a una condena de tres años de prisión para el genetista He JianKui por “práctica ilegal de la medicina”.

Fotografía del científico Je JianKui durante la presentación en el congreso de edición genética en noviembre de 2018, de su experimento en humanos
Sin embargo, este suceso solo nos deja un montón de interrogantes y abrió una caja de pandora, cuyas consecuencias son impredecibles para la humanidad.
Ahora bien, ¿Qué tiene que ver este suceso con las vacunas RNAm?. Empecemos:
Los hechos
La tecnología de edición genética CRISPR con la que se editó los genes de estos bebes, es una tecnología todavía en experimentación. CRISPR actúa como unas “tijeras moleculares” que cortan el ADN con la posibilidad de introducir cambios en el mismo.
El objetivo del Dr. JianKui era volver a estas gemelas resistentes a la infección del VIH, esto lo hizo “cortando” el gen CCR5 que codifica un receptor celular, por donde entra el VIH.
Pero el problema es que, por un lado, la especificidad de estas tijeras moleculares no es absoluta, y CRISPR puede terminar cortando el ADN en otras áreas en donde no se pretendía modificar, con consecuencias imprevisibles.
Y, por otro lado, los daños colaterales al realizar cambios genéticos no se han dimensionado en su totalidad, para seguir con éste ejemplo real, el receptor que codifica el gen CCR5 es necesario para que las células humanas se defiendan de virus de la influenza.
Por lo tanto, esta modificación genética realizada por el Dr. He JianKui dejó expuestas a estas gemelas a infecciones más graves de la gripe. En conclusión, es probable que no mueran de SIDA, pero sí las puede matar una simple gripe.
Aspectos éticos
La justicia china catalogó al Dr. He JianKui como un “lobo solitario en busca de gloria”, sin embargo, este suceso dejó muchos interrogantes que aún están en el ambiente:
¿De dónde vino la financiación para la experimentación ilegal de JianKui?
¿Cómo es posible que el Dr JianKui se haya podido saltar todos los controles y haber llevado a término esta investigación con humanos?
¿Qué otros experimentos con humanos se están realizando, sin que el mundo lo sepa?
Indistintamente de las motivaciones que este científico haya tenido, está claro que los aspectos regulatorios y de control deben ser más efectivos para que una herramienta científica con tanto potencial no se convierta en una bomba atómica.
La capacidad de cambios de esta herramienta en el cuerpo y la mente humana son ilimitados, esta tecnología tiene el potencial de “fabricar” superhumanos, una nueva raza superior sin deficiencias genéticas, con mayor fortaleza física y mejores capacidades intelectuales.
Por otro lado, también tiene el potencial de todo lo contrario, de crear monstruos. En sociedades permisivas, en donde el “libre desarrollo de la personalidad” es un derecho fundamental, en esas comunidades en las que ocurren cosas inverosímiles como, por ejemplo, que un influencer se implante senos, las posibilidades de deformidad también pueden ser ilimitadas.
Se abre una esfera de posibilidades para la humanidad de aquí en adelante, dependiendo del uso que le demos a esta herramienta.
Aspectos Moleculares
El DNA (Deoxyribonucleic Acid) guarda toda la información genética y está ubicado en el núcleo de cada célula humana. Hay tres procesos que la célula realiza con su material genético:
Replicación.
Consiste en duplicación del material genético para que la célula pueda reproducirse y crear dos nuevas células a partir de una unidad, éste proceso se realiza en el núcleo de la célula. La capacidad de replicación celular va a depender del tipo de tejido, así, por ejemplo, la piel y las mucosas tienen un alto índice de replicación a diferencia del tejido nervioso o cardíaco en que la replicación es menor.
Transcripción.
Los genes guardan la información, pero las moléculas encargadas de la ejecución de esa información son las proteínas, y el intermediario en este proceso es el RNA mensajero (RNAm). Éste proceso también se realiza en el núcleo celular.
Una vez se forma el RNAm a partir del DNA, el primero sale al citoplasma de la célula para ahora sí crear las proteínas.
Traducción.
Hay que tener en cuenta que RNA hay varios, pero los más importantes son el RNA mensajero del que ya hablamos y los RNA de transferencia y RNA ribosomales, estos dos últimos son los encargados del ensamble de los aminoácidos que constituyen las proteínas.
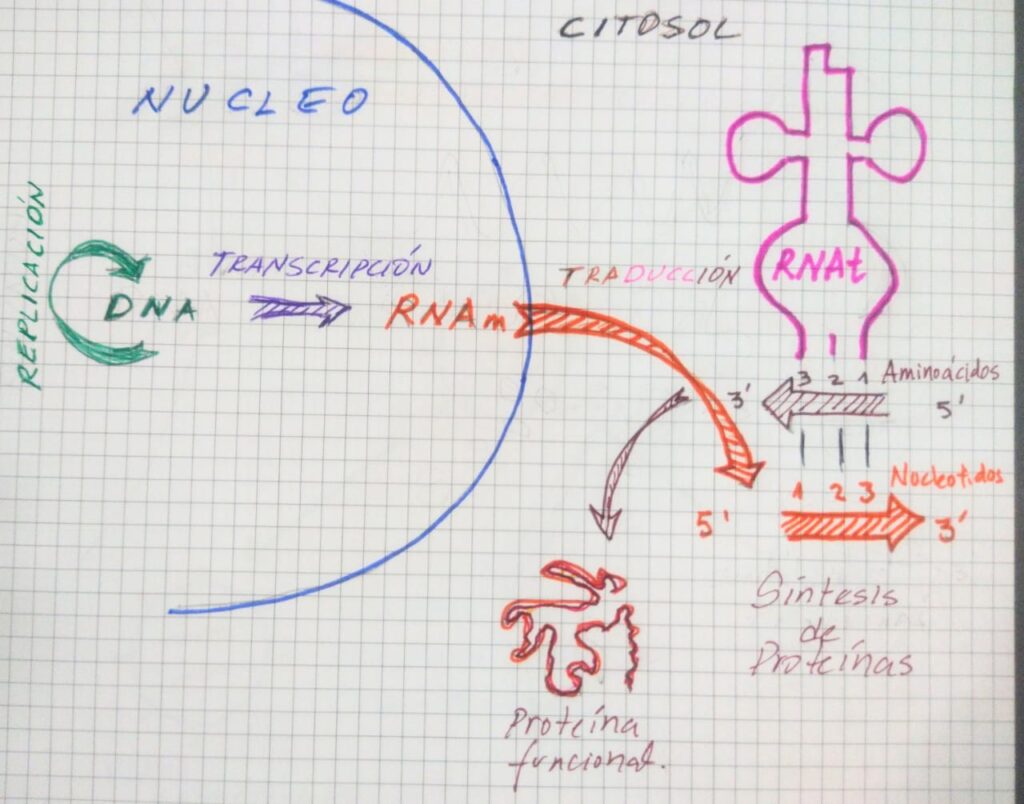
Imagen de los procesos de Replicación de ADN necesario para la división celular, Transcripción en el que la información genética es pasada al RNA mensajero (RNAm), que luego sale del núcleo al citoplasma y junto con la maquinaria de RNA ribosomal (RNAr) y en RNA de transferencia (RNAt) ensamblan los aminoácidos en tripletas para formar las proteínas funcionales. Fuente. Elaboración propia.
Este principio emplea la vacuna de RNAm, inyecta la información genética de la proteína S del SARS-Cov-2, para que la misma maquinaria de la célula sintetice la proteína, y se genere una respuesta inmune ante el virus.
Pero este mismo principio puede ser empleado para tratar otro tipo de enfermedades que no necesariamente son de etiología infecciosa. En un futuro se podrá inyectar RNAm para sintetizar proteínas que ciertas personas no sintetizan y que son causas de enfermedades.
Eventualmente, enfermedades causadas por mutaciones genéticas de un solo nucleótido (SNPs) podrían ser tratadas por este método, verbigracias Síndrome de Dravet, Síndrome de Angelman y muchos otros. No obstante, tendría limitaciones para tratamiento de enfermedades cuya etiología sea multigénica (causada por varios genes) por ejemplo enfermedades neurodegenerativas como la demencia tipo Alzheimer, el Parkinson y la Esclerosis Lateral Amiotrófica.
Ingeniería de Edición Genética
Lograr todos estos avances en ingeniería genética ha sido el resultado de miles de investigaciones y desarrollo científico, en efecto el premio Nobel de química del año 2020 fue otorgado a dos investigadoras Jenifer Doudna y Emanuelle Charpentier, por investigaciones en éste campo.
La herramienta más poderosa de edición genética es CRISPR (Clustered Regularly Interespaced Short Palindromic Repeat).
Desde finales del siglo pasado a muchos científicos les llamó la atención que muchas bacterias y arqueas tenían códigos genéticos virales incrustados dentro de su propia información genética (CRISPR), y no fue hasta éste siglo que se logró identificar la razón de dicho hallazgo.
Esas bacterias y arqueas tienen un sistema avanzado de respuesta inmune, en el que incorporan el código genético de virus invasores a su propio código para tener una memoria del mismo y poder reconocerlo e inactivarlo en una próxima invasión.
Para eso se vale de proteínas que forman el complejo CRISPR-Cas, de estas se han detectado seis tipos:
- Tipo I – Cas3
- Tipo II – Cas9
- Tipo III – Cmr complex
- Tipo IV – Todavía desconocida
- Tipo V – Cas 12
- Tipo VI – Cas 13
Vídeo Explicativo del funcionamiento de CRISPR – Cas9. Fuente MIT Institute.
Conclusión
Los científicos utilizaron la misma herramienta de corte molecular que por milenios han utilizado las bacterias para defenderse de los virus. El sistema tipo II es el más estudiado (CRISPR- Cas 9), la razón es porque puede ser artificialmente programada para manipular genes en organismos vivos, el ser humano dentro de ellos. Sin embargo, es una tecnología que se encuentra en pañales y que sin lugar a dudas cambiará el mundo en que vivimos.
Bibliografía
Morris, G., Maes, M., Berk, M., & Puri, B. K. (2019). Myalgic encephalomyelitis or chronic fatigue syndrome: how could the illness develop? In Metabolic Brain Disease (Vol. 34, Issue 2, pp. 385–415). Springer New York LLC. https://doi.org/10.1007/s11011-019-0388-6
Rosenberg´s Molecular and Genetic Basic of Neurological and Psychiatric Disease (2019). Sixth Edition. Ed Academic Press Elsevier.
Xu, S., Yang, K., Li, R., & Zhang, L. (2020). Mrna vaccine era—mechanisms, drug platform and clinical prospection. In International Journal of Molecular Sciences (Vol. 21, Issue 18, pp. 1–35). MDPI AG. https://doi.org/10.3390/ijms21186582
Identifican el papel del receptor CCR5 en la formación de anticuerpos y memoria inmune tras la vacunación






