
Durante siglos, la medicina se centró únicamente en el cuerpo humano como un sistema cerrado. Hoy, la ciencia nos revela que somos un vasto ecosistema.
Mientras que la microbiota corresponde a todos los microorganismos que residen en nuestro cuerpo, el microbioma, es un concepto más general que incluye su entorno, la colección de su material genético y los metabolitos que producen.
El microbiota que habita en el intestino humano comprende varios microorganismos incluidos bacterias, virus, arqueas, bacteriófagos y protozoos.
Este ecosistema complejo es crucial para moldear la homeostasis humana y nuestra susceptibilidad a las enfermedades. Entender cómo funciona este universo interno es fundamental, ya que su estado de equilibrio (eubiosis) o desequilibrio (disbiosis) es un factor determinante en trastornos que van desde la fatiga crónica y las migrañas hasta la diabetes tipo 2 y el Alzheimer.
Una Breve Historia: De Pequeños Animales al Órgano Virtual.
Los conceptos sobre la existencia de microorganismos en el cuerpo se remontan a los «pequeños animales» observados por Leeuwenhoek. Siglos más tarde, Pasteur y Koch sentaron las bases para comprender la causalidad microbiana de las enfermedades infecciosas.
A principios del siglo XX, Ilya Metchinikov, un microbiólogo ruso, fue el primero en vincular la microbiota intestinal con la salud humana, en honor a este científico se desarrollo uno de los probióticos más completos del mercado, el Metchniprob.
El conocimiento sobre el microbioma se disparó rápidamente en el siglo XXI. La aplicación de técnicas de secuenciación de ADN de última generación (NGS) en la década de 2000, junto con estrategias computacionales avanzadas, permitió por primera vez identificar, cultivar y estudiar las complejas comunidades microbianas, incluyendo las que habitan en el tracto gastrointestinal (GI).
Figura 1. Fotografía representativa Luis Pausteur en su laboratorio. Fuente: Generada por IA.

Los Múltiples Ecosistemas: Tipos de Microbiota.
La microbiota no reside solo en el intestino; coloniza establemente diversas mucosas y nichos ecológicos.
Tabla 1. Características y localización de la microbiota humana.
Tipo de Microbiota | Características y Localización | Concentración y Géneros Clave |
Oral (Boca) | Integra más de 700 especies variables (lengua, saliva, encías, placa dental). Es influida por la dieta y la higiene. | Muy alta: 10^8 – 10^9 bacterias/ml. Géneros como Streptococcus, Actinomyces, Candida. Sus alteraciones se vinculan con periodontitis e inflamación sistémica. |
Gastrointestinal (Intestino) | El ecosistema más abundante y diverso. Varía su concentración drásticamente desde el estómago (pH 1-2 , baja concentración hasta el colon (densidad de $10^11 – 10^12$ bacterias/ml). | Dominada por los filos Firmicutes y Bacteroidetes (90%) en adultos sanos. |
Vaginal | Dominada por especies de Lactobacillus. Estos son esenciales para mantener un pH ácido protector (alrededor de 4.5). | Lactobacillus crispatus, L. iners, etc. La disminución de Lactobacillus se asocia con vaginosis bacteriana. |
Cutánea (Piel) | Presente en toda la piel. Varía con la humedad, la temperatura y los productos tópicos aplicados. Desempeña funciones importantes en la defensa de la barrera cutánea. | Varía (ej. Staphylococcus, Corynebacterium). |
Pulmonar | Aunque con un recuento microbiano menor que el intestino, forma parte del microbioma humano y está involucrada en la homeostasis respiratoria. | Diversidad baja, distinta a la intestinal. |
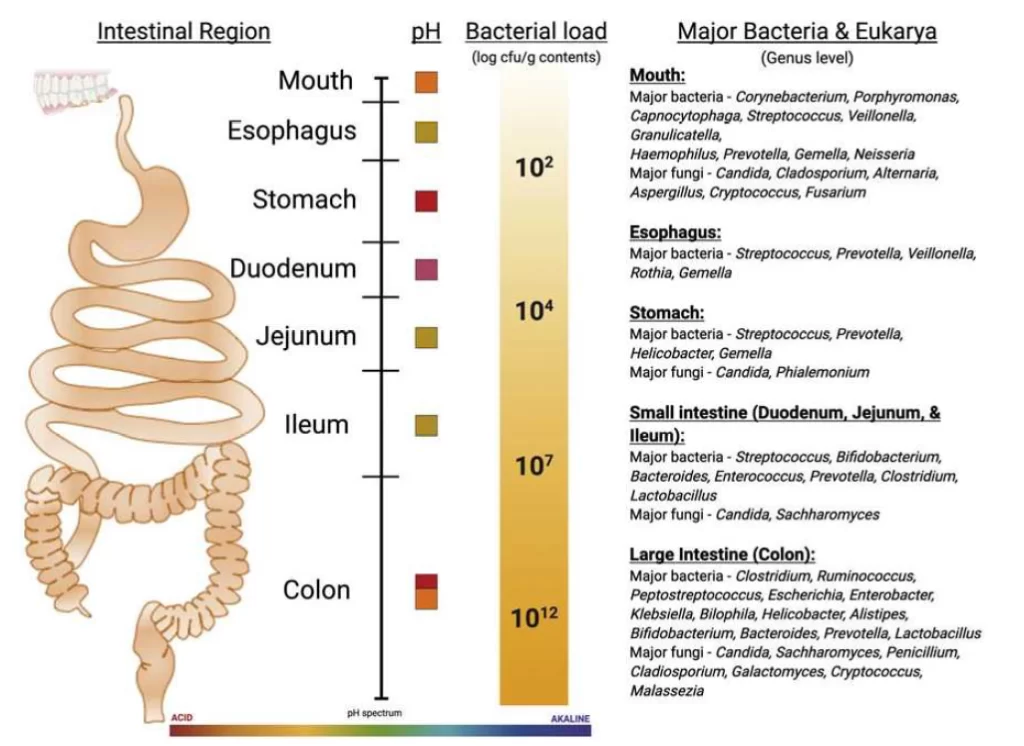
Imagen 2. Microbiota en el sistema digestivo. Fuente: Marriott, 2023.
Funciones Vitales de la Microbiota Intestinal.
Las funciones de la microbiota intestinal son tan extensas que se le atribuyen más de 300 funciones.
- Protección y Defensa de la Mucosa: Refuerza y protege la mucosa intestinal. Mantiene la integridad de la barrera epitelial. También genera sustancias antimicrobianas que defienden contra patógenos.
- Facilitación de Nutrición y Digestión: Facilita la digestión y absorción de nutrientes. Es esencial para la fermentación de carbohidratos no digeribles (fibra) y almidón resistente.
- Síntesis de Vitaminas Esenciales: Produce vitaminas cruciales que el huésped no puede sintetizar, incluyendo la Vitamina K2, y varias vitaminas del Complejo B (B1, B2, B3, B5, B6, B9/Folato, B12/Cobalamina).
- Modulación Inmunitaria: Entrena y modula el sistema inmune intestinal, promoviendo la tolerancia inmune y regulando la inflamación.
- Regulación Metabólica: Influye en el metabolismo y el peso, particularmente a través de la producción de metabolitos clave (AGCC).
- Eje Intestino-Cerebro: Modula la función cerebral, ya que produce neurotransmisores como GABA y serotonina.
- Metabolismo de Tóxicos: Participa en el metabolismo de los metales pesados, ya sea secuestrándolos o alterando su solubilidad mediante la modulación del pH intestinal.
Los Protagonistas: Bacterias Intestinales Clave.
Aunque hay más de 1150 especies bacterianas por persona, algunos grupos funcionales son vitales:
Tabla 2. Microbiota intestinal con sus principales beneficios.
Grupo Funcional | Bacterias Representativas | Rol Clave |
Protectora | Bacteroides spp., Bifidobacterium spp., Lactobacillus spp. | Defensa, producción de ácido láctico y H₂O₂. |
Muconutritiva | Akkermansia muciniphila | Degradación de mucina, estimula la producción de nueva capa mucosa, fortaleciendo las uniones estrechas (tight junctions). |
Productora de ácidos grasos de cadena corta | Faecalibacterium prausnitzii, Roseburia spp. | Principal productor de Butirato en el colon. |
Fermentadora | Ruminococcus bromii | Rompe cadenas complejas de fibra y almidón resistente para alimentar a las productoras de butirato. |
Neuroactiva | Bifidobacterium, Lactobacillus plantarum, Escherichia coli (comensales) | Producción de neurotransmisores (GABA, Serotonina, Dopamina). |
El Poder de los Posbióticos: Los Mensajeros Químicos.
Los posbióticos son los metabolitos bioactivos que produce la microbiota y que actúan como señales para el huésped. El grupo más estudiado son los Ácidos Grasos de Cadena Corta (SFCAs), derivados de la fermentación de la fibra.
Tipos y Funciones de los AGCC:
Butirato:
Función Metabólica/Inmunológica: Es la principal fuente de energía para los colonocitos. Refuerza la integridad de la barrera epitelial y reduce la permeabilidad intestinal. Es un potente antiinflamatorio (inhibe NF-κB, IL-6, IL-1) y favorece la apoptosis de células tumorales. Además, mejora la sensibilidad a la insulina y el control glucémico.
Propionato:
Función Metabólica: Se absorbe en el hígado, donde inhibe la síntesis de colesterol y contribuye al metabolismo de la glucosa. También tiene un efecto saciante al estimular hormonas PYY y GLP-1.
Acetato:
Función General: Es el AGCC más abundante. Sirve como fuente de energía para tejidos periféricos y el cerebro y apoya la producción de mucina.
Otro Metabolito Clave: TMAO
La microbiota también produce metabolitos potencialmente dañinos si se descontrolan. Las bacterias proteolíticas, como Clostridium, Desulfovibrio y Proteus, convierten la colina y la L-carnitina de la dieta en trimetilamina (TMA).
El hígado oxida la TMA a óxido de trimetilamina (TMAO), un factor de riesgo para enfermedades cardiovasculares y aterosclerosis.
El butirato juega un papel protector aquí, ya que reduce la formación de TMAO al suprimir las enzimas bacterianas productoras de TMA y fortalecer la barrera intestinal, limitando el paso de TMA a la circulación portal.
Interacciones Microbianas y el Concepto de Cross-Feeding.
La microbiota no funciona de forma aislada. Las comunidades microbianas interactúan entre sí a través de un mecanismo conocido como alimentación cruzada (cross-feeding).
Un ejemplo clásico es: las bacterias fermentadoras primarias, como las Bifidobacterium, producen subproductos como el lactato y el acetato a partir de la fibra dietética. Estas moléculas son luego utilizadas por bacterias butirogénicas, como Faecalibacterium y Roseburia, para producir el beneficioso butirato.
Además, el viroma (virus bacteriófagos) actúa regulando el bacterioma, asegurando un equilibrio dinámico al controlar la proliferación de bacterias.
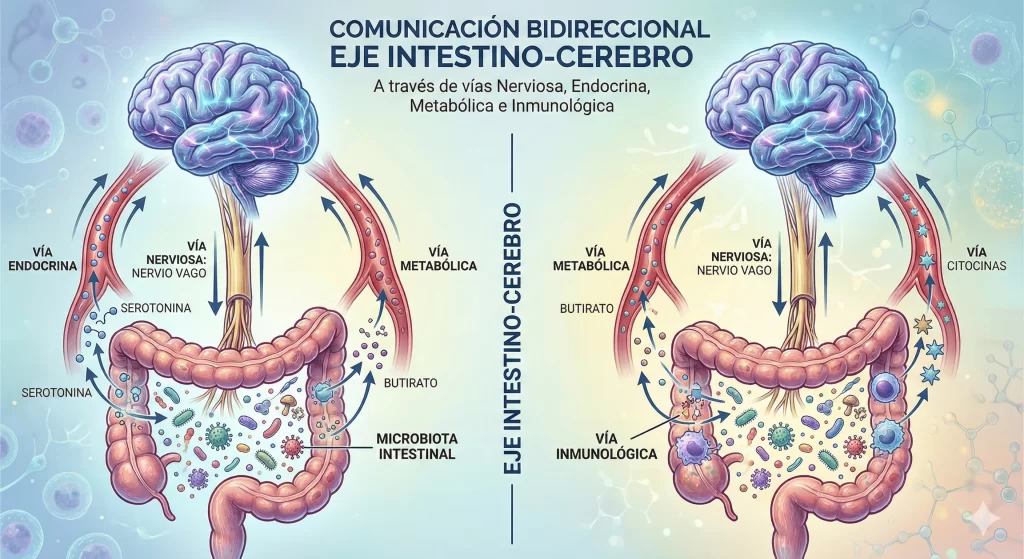
Imagen 3. Infografía que revela la comunicación bidireccional del eje intestino cerebro a través de la vía nerviosa (nervio vago), vía metabólica (metabolitos como el butirato), vía endocrina y vía inmunológica a través de citocinas. Elaboración propia.
Disbiosis: El Desequilibrio y las Enfermedades.
La disbiosis es un desequilibrio cualitativo y/o cuantitativo de la microbiota en un nicho ecológico. Este estado se ha asociado con la «epidemia silenciosa de desnutrición crónica oculta» y la proliferación de síntomas sistémicos y trastornos metabólicos.
Tabla 3. Bacterias de la microbiota y su relación con algunas enfermedades.
Enfermedad/Trastorno | Variación de la Microbiota Clave | Mecanismo Fisiopatológico |
Enfermedad Inflamatoria Intestinal (EII) (Crohn, Colitis Ulcerosa) | Reducción drástica de Faecalibacterium prausnitzii y Roseburia. | Disminución de butirato → pérdida de protección de la mucosa e inflamación crónica. |
Obesidad/Diabetes T2 | Reducción de Akkermansia muciniphila y Bifidobacterium. | Endotoxemia Metabólica: Aumento de la permeabilidad intestinal (zonulina alta) → paso de lipopolisacáridos (LPS) bacterianos a la sangre → inflamación crónica de bajo grado → resistencia a la insulina. |
Trastornos Neurológicos (Alzheimer, Parkinson, Autismo, Depresión) | Alteración de bacterias neuroactivas y aumento de productores de toxinas. | Hiperpermeabilidad de la Barrera Hematoencefálica (BHE) y translocación de LPS y metales pesados. |
Cáncer Colorrectal | Aumento de bacterias proteolíticas (Clostridium spp.) y Fusobacterium nucleatum. | Producción de metabolitos tóxicos (amoníaco, fenoles, indoles). |
SIBO (Sobrecrecimiento Bacteriano del Intestino Delgado) | Proliferación excesiva de bacterias del colon (ej. E. coli, Klebsiella) en el intestino delgado. | Causado por hipoclorhidria (uso de IBP), falla del Complejo Motor Migratorio (CMM), o uso de opioides. Puede producir exceso de H₂, CH₄ (metano, asociado a estreñimiento severo) o H₂S (sulfuro de hidrógeno). |
Prebióticos: Alimentando a sus Aliados.
Para mantener la eubiosis y el equilibrio, necesitamos suministrar prebióticos, que son sustratos dietéticos no digeribles y fermentables que estimulan selectivamente el crecimiento de microorganismos beneficiosos (fibra).
Los principales prebióticos incluyen:
- Fibra Dietética y Carbohidratos Saludables: Sustratos esenciales para que la microbiota produzca AGCC (butirato, propionato, acetato).
- Almidón Resistente: Un tipo de carbohidrato fermentado por bacterias clave como Ruminococcus bromii.
- Oligosacáridos (FOS, GOS): Favorecen específicamente a géneros beneficiosos como Bifidobacterium y Lactobacillus.
- Polifenoles: Compuestos presentes en vegetales y frutas.
- Oligosacáridos de la Leche Humana (HMOs): Cruciales en la lactancia, ya que alimentan a Bifidobacterium infantis, determinando la composición adulta de la microbiota.
Al igual que un jardín necesita la tierra adecuada para florecer, su microbiota necesita prebióticos específicos para producir los posbióticos (butirato, acetato, propionato) que mantienen su cuerpo sano, sus defensas fuertes y su mente clara. Cuidar su microbioma es, en esencia, cuidar su salud integral.
Conclusión.
El microbioma intestinal, reconocido como un «órgano» vital por su vasta capacidad metabólica, moldea profundamente la homeostasis humana y nuestra susceptibilidad a las enfermedades.
Este ecosistema es crucial, no solo por su papel en la digestión y la síntesis de vitaminas esenciales (K2, Complejo B), sino también por la producción de posbióticos fundamentales como el butirato, la principal fuente de energía de los colonocitos que protege la barrera intestinal y modula la inflamación.
La pérdida de este equilibrio (disbiosis) se relaciona con la «desnutrición crónica oculta» y la proliferación de síntomas sistémicos y trastornos neuropsiquiátricos.
La exposición a agresores, como la gliadina o ciertas bacterias, activa la zonulina, desencadenando la aumento de la permeabilidad intestinal. Esta «fuga» permite que toxinas como los lipopolisacáridos (LPS) ingresen a la circulación, iniciando la endotoxemia metabólica y la inflamación crónica sistémica, la cual es la base de enfermedades metabólicas (obesidad, diabetes) y neurodegenerativas.
El objetivo de la ciencia es aprovechar esta diversidad. Cuidar la microbiota mediante prebióticos y la suplementación de nutrientes que fortalecen la barrera intestinal (Zinc, Glutamina, Vitamina D) es indispensable para restaurar las defensas y lograr una salud integral y sostenible.
Doctor Andrés Naranjo Cuéllar.
Médico y Cirujano.
MSc en Nutrición.

Bibliografía.
Cani, P. D., Amar, J., Iglesias, M. A., Poggi, M., Knauf, C., Bastelica, D., … & Pralong, F. P. (2007). Metabolic endotoxemia initiates obesity and insulin resistance. Diabetes, 56(7), 1761-1772.
DiNicolantonio, J. J., O’Keefe, J. H., & Wilson, W. (2018). Subclinical magnesium deficiency: a principal driver of cardiovascular disease and a public health crisis. Open Heart, 5(1), e000668.
Fasano, A. (2011). Zonulin and its regulation of intestinal barrier function: the biological door to inflammation, autoimmunity, and cancer. Physiological Reviews, 91(1), 151-175.
Fasano, A. (2012). Leaky gut and autoimmune diseases. Clinical Reviews in Allergy & Immunology, 42(1), 71-78. https://pubmed.ncbi.nlm.nih.gov/22109896/
Kalkan, A. E., BinMowyna, M. N., Raposo, A., Ahmad, M. F., Ahmed, F., Otayf, A. Y., … & Karav, S. (2025). Beyond the Gut: Unveiling Butyrate’s Global Health Impact Through Gut Health and Dysbiosis-Related Conditions: A Narrative Review. Nutrients, 17(8), 1305. https://pubmed.ncbi.nlm.nih.gov/40284169/
Langan, R. C., & Goodbred, A. J. (2017). Vitamin B12 Deficiency: Recognition and Management. American Family Physician, 96(6), 384-389. https://pubmed.ncbi.nlm.nih.gov/28925645/
Marriot, P. (2023) Present Knolwledge in nutrition. 11 Ed. Ed. Elsevier.
Mechlińska, M., Kaczmarek, B., Skonieczna, A., & Mechliński, M. (2025). The Interplay between Small Intestinal Fungal Overgrowth (SIFO) and Co-Occurring Gastrointestinal Disorders—A Narrative Review. Nutrients, 17(2), 487. https://pubmed.ncbi.nlm.nih.gov/25786900/
Mu, Q., Kirby, J., Reilly, C. M., & Luo, X. M. (2017). Leaky gut as a danger signal for autoimmune diseases. Frontiers in Immunology, 8, 598. https://pubmed.ncbi.nlm.nih.gov/28588585/
Pierre, J. F., & Leone, V. A. (2020). The Microbiome and Health. In Present Knowledge in Nutrition (pp. 605-624). Elsevier.
Takakura, W., & Pimentel, M. (2020). Small Intestinal Bacterial Overgrowth and Irritable Bowel Syndrome—An Update. Frontiers in Psychiatry, 11, 664. https://pubmed.ncbi.nlm.nih.gov/32754068/
Turnbaugh, P. J., Ley, R. E., Mahowald, M. A., Magrini, V., Mardis, E. R., & Gordon, J. I. (2006). An obesity-associated gut microbiome with increased capacity for energy harvest. Nature, 444(7122), 1027-1031. https://pubmed.ncbi.nlm.nih.gov/17183312/







