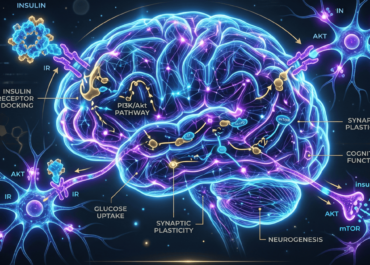
Introducción al Eje Intestino-Cerebro (GBA [Gut-Brain Axis]).
La microbiota intestinal se define como la comunidad diversa de microorganismos (bacterias, arqueas, virus, hongos y protozoos) que residen en el tracto gastrointestinal humano. Esta comunidad desempeña un papel crucial en la digestión, absorción de nutrientes, producción de vitaminas y regulación del sistema inmunológico.
El concepto del eje intestino-cerebro (GBA) describe una vía de comunicación bidireccional que integra las funciones emocionales y conductuales con la inmunidad y el metabolismo sistémico. Las alteraciones en este equilibrio, conocidas como disbiosis, se han vinculado no solo con trastornos metabólicos como la obesidad y la diabetes, sino también con diversas patologías psiquiátricas y neurológicas.
Vías de Comunicación Bidireccional
El GBA opera a través de cuatro vías principales que permiten la señalización constante entre el lumen intestinal y el sistema nervioso central (SNC) (Nutrition and Psychiatric Disorders. An Evidence-Based Approach to Understanding the Diet-Brain connection, 2024).:
Vía Neural (Nervio Vago):
El nervio vago actúa como una «autopista» de información que conecta el tronco encefálico con el sistema digestivo. El 80-90% de sus fibras son aferentes, enviando señales sobre el estado metabólico y la presencia de compuestos químicos desde el intestino al cerebro.
Imagen 1. Inervación del nervio vago. Fuente:(Moore, Keith, 1985/1985).

Vía Hormonal (Eje HPA):
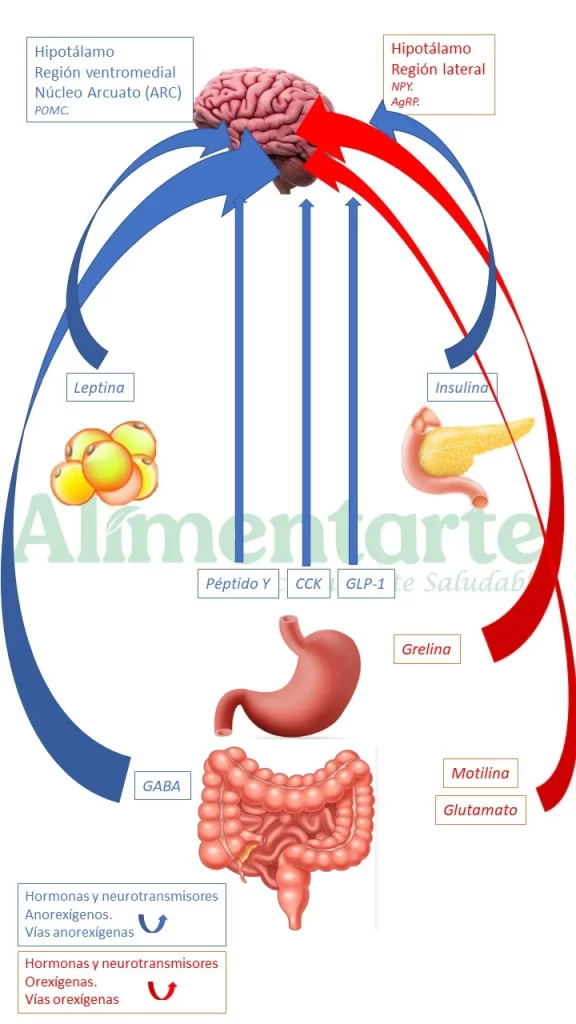
El eje hipotálamo-pituitario-adrenal regula la respuesta al estrés mediante la liberación de cortisol, CRH y ACTH. La disbiosis puede hiperactivar este eje, exacerbando condiciones de ansiedad y depresión. Además, la microbiota influye en la producción de neurotransmisores como la serotonina (5-HT), dopamina y GABA y el control del ciclo hambre saciedad.
Imagen 2. Vías de comunicación hormonal en el eje intestino cerebro, en azul vías y neurotransmisores orexígenos (saciantes) y en rojo anorixigenos (hambre). Fuente: elaboración propia.
Vía Inmunológica (Citoquinas):
Las células inmunes intestinales liberan citoquinas (como IL-1, IL-6 y TNF-α) en respuesta a la inflamación o infección, las cuales pueden cruzar la barrera hematoencefálica y afectar las funciones cognitivas y emocionales.
Vía Metabólica (Ácidos Grasos de Cadena Corta – SCFAs):
Los SCFAs, como el acetato, butirato y propionato, son subproductos de la fermentación bacteriana de la fibra dietética. Estos metabolitos pueden cruzar la barrera hematoencefálica, modular la homeostasis de la microglía y fortalecer la integridad de la barrera epitelial.
Fisiopatología de la Disbiosis y Síndrome Metabólico (MetS).
La inflamación crónica de bajo grado es la base fisiopatológica del MetS. Una ruptura en la barrera intestinal permite la translocación de lipopolisacáridos (LPS) y otros metabolitos bacterianos al torrente sanguíneo, desencadenando una respuesta inflamatoria sistémica denominada endotoxemia metabólica.
Obesidad y Diabetes Tipo 2:
Se han observado diferencias sustanciales en la composición de la microbiota entre individuos sanos y obesos, con alteraciones significativas en géneros como Akkermansia y Faecalibacterium y un incremento del Enterobacter cloacae. Estudios en ratas Zucker mostraron que la progresión hacia la diabetes se asocia con un aumento de bacterias patogénicas y una disminución de productoras de butirato (Hefnawy, 2024).
Dislipidemia e Hipertensión:
La microbiota explica hasta el 6% de la variación en los triglicéridos y el 4% en el HDL. Dietas altas en fructosa o glucosa reducen la diversidad microbiana, aumentando la relación de Proteobacteria.
Hígado Graso No Alcohólico (NAFLD):
El desarrollo de NAFLD está fuertemente influenciado por metabolitos bacterianos que atraviesan la barrera intestinal, activando de forma inapropiada el sistema inmune a través del eje enterohepático.
Impacto en Trastornos Psiquiátricos Específicos.
Depresión Mayor (MDD):
Los pacientes con MDD presentan niveles significativamente menores de Bifidobacterium y Lactobacillus. La inflamación sistémica y el estrés oxidativo se han identificado como mecanismos clave que contribuyen al declive cognitivo en estos pacientes (McGuinness et al., 2022).
Ansiedad:
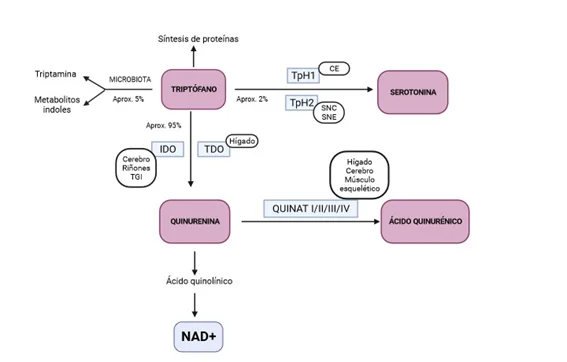
Estudios preclínicos demuestran que la microbiota modula la respuesta al miedo. Por otro lado, el desvío del metabolismo del triptófano en favor de la vía de la quinurenina en lugar de la formación de serotonina, se ha relacionado con ansiedad y depresión.
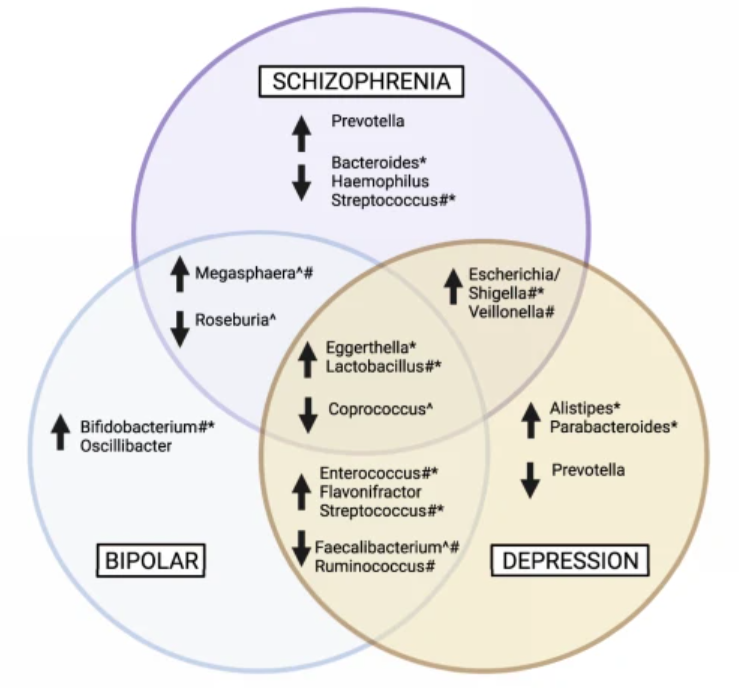
Los niveles reducidos de Faecalibacterium y Coprococcus , así como los niveles elevados de Eggerthella se encontraron en ansiedad, depresión y esquizofrenia (Nikolova et al., 2021).
Imagen 3. Vías del metabolismo del triptófano hay tres vías principales, formación de serotonina arriba derecha, la vía de los indoles (específicamente por la microbiota intestinal) y la vía de la quinurenina abajo. Fuente: (Chicharro, 2023).
Trastorno del Espectro Autista (ASD):
Los individuos con ASD tienen una mayor prevalencia de problemas digestivos debidos a una composición microbiana anormal. Se postula que la disbiosis afecta el desarrollo cerebral a través de la síntesis alterada de metabolitos y neurotransmisores, además de una posible deficiencia de vitamina B6 mediada por la microbiota.
Esquizofrenia:
Se ha propuesto que la microbiota influye en el ciclo glutamato-glutamina-GABA y se ha observado una fisiopatología similar entre la esquizofrenia y la obesidad, sugiriendo la disbiosis como una raíz común (McGuinness et al., 2022).
Imagen 4. Esquema que muestra la alteración de la microbiota en Depresión Mayor, Trastorno Afectivo Bipolar y Esquizofrenia. Fuente:(McGuinness et al., 2022)
Nutricion en la Salud Mental.
La dieta es el modulador más potente de la microbiota, capaz de inducir cambios significativos en solo 24 horas.
las dietas con ricas en azúcares, grasas saturadas y ultraprocesados se asocian con un mayor riesgo de depresión y ansiedad. Por el contrario, los ácidos grasos Omega-3 (EPA y DHA) reducen las citoquinas proinflamatorias y mejoran los resultados en salud mental.
Tabla 1. Marcadores inflamatorios en enfermedades mentales. Fuente: modificado de (Yuan et al., 2019).
| IL-2 | IL-2R | IL-4 | IL-6 | IL-6R | PCR | BDNF |
Depresión |
|
|
| ↑ |
| ↑ | ↓ |
TAB |
| ↑ | ↑ |
|
|
|
|
SEPT |
| ↔ |
|
|
|
|
|
Suicidio | ↓ |
| ↓ | ↑ |
| ↑ |
|
TS |
|
|
| ↑ |
| ↑ |
|
Esquizofrenia |
|
|
| ↑ |
| ↑ | ↓ |
Una dieta rica en frutas, vegetales y frutos secos puede contrarrestar los efectos de los Radicales Libres de Oxígeno (ROS) que se han encontrado elevados en varias enfermedades mentales.
Por otro lado, la falta de nutrientes específicos tiene manifestaciones psiquiátricas directas. Por ejemplo, la deficiencia de niacina (B3) se vincula con demencia; la de tiamina (B1) con el síndrome de Wernicke-Korsakoff; y la de zinc y folato con depresión y defectos del tubo neural.
Existe una asociación significativa entre la intolerancia al gluten y trastornos como TDAH, ansiedad y depresión. Los anticuerpos antigliadina (AGA) pueden reaccionar de forma cruzada con proteínas sinápticas, sugiriendo un mecanismo de disfunción neurológica mediada por el sistema inmune.
Intervenciones Terapéuticas Basadas en la Microbiota.
- Probióticos: Microorganismos vivos que, en cantidades adecuadas, confieren beneficios a la salud. Cepas como L. rhamnosus y Bifidobacterium longum han mostrado reducir síntomas de ansiedad y depresión en ensayos clínicos. En adultos mayores, probióticos como B. bifidum BGN4 han mejorado la función cognitiva y mitigado el estrés mental.
- Prebióticos: Sustancias no digeribles que estimulan selectivamente el crecimiento de bacterias beneficiosas. Los oligosacáridos de la leche humana (HMO), FOS y GOS han demostrado efectos ansiolíticos y antiinflamatorios.
- Psicobióticos: Un término emergente para referirse a probióticos, prebióticos y otras terapias dirigidas a la microbiota que benefician la salud mental.
- Trasplante de Microbiota Fecal (FMT): Utilizado inicialmente para infecciones por C. difficile, el FMT está siendo investigado para tratar el MetS, la diabetes tipo 2 y síntomas de ASD. No obstante, existen preocupaciones sobre la seguridad y la transmisión de patógenos multirresistentes.
Tabla 2. Investigaciones con los efectos de diferentes psicobióticos. TEA, Trastorno del Espectro Autista; ATEC, Lista de Chequeo para el Tratamiento del Autismo; BDI, Puntuación de Depresión de Beck; ADHD, Síndrome de Déficit de Atención e Hiperactividad.
Psicobióticos. | Efecto en la salud mental. | Modelo del estudio. | Referencia. |
L. acidophilus, L. rhamnosus, B. longum. | Significativo mejoramiento de los síntomas de pacientes autistas. Escala ATEC | 30 niños con TEA entre 5 y 9 años | (Shaaban et al., 2018) |
L. helveticus, B. longum | Mejoría de los síntomas de depresión. Escala BDI. | 110 adultos con Depresión mayor. | (Kazemi et al., 2019) (Wallace & Milev, 2021) |
L. acidophilus, L. casei, B. longum | Mejoría de los síntomas de depresión. | 40 pacientes con Depresión mayor | (Akkasheh et al., 2016) |
L. acidophilus, L. reuteri, L. fermentum | Mejoría de los síntomas de Esquizofrenia. | 60 pacientes con Esquizofrenia crónica. | (Ghaderi et al., 2019) |
B. longum, B. bififum, B. lactis, L acidophilus | Disminución de los síntomas de ansiedad. | 48 pacientes con diagnóstico de trastorno de ansiedad. | (Eskandarzadeh et al., 2021) |
B. bifidum | Mejora de la atención, y reducción de la impulsividad e hiperactividad. | 30 niños con diagnóstico de ADHD. | (Wang et al., 2022) |
B. bifidum, B. longum | Mejoría de funciones cognitivas y nivel de depresión. | 63 adultos saludables, mayores de 64 años. | (Kim et al., 2021) |
B. bifidum, B. lactis, B. longum, B. acidopholus | No mejoría en pacientes con TAB | 38 pacientes con TAB tipo I | (Eslami Shahrbabaki et al., 2020) |
Consideraciones Clínicas: Dosificación y Seguridad.
La eficacia de los probióticos es dependiente de la cepa, la dosis y la especificidad del paciente.
- Dosificación: Algunos estudios sugieren que dosis superiores a 10^9 o 10^10 UFC/día son más efectivas para tratar la diarrea asociada a antibióticos y reducir la presión arterial. En niños autistas, dosis de 100×10^6 UFC de diversas cepas durante 12 semanas mejoraron significativamente las puntuaciones ATEC.
- Seguridad: Aunque generalmente seguros, se han reportado casos raros de bacteriemia, endocarditis y sepsis neonatal asociados al uso de probióticos en pacientes inmunocomprometidos o gravemente enfermos, y en neonatos se han reportado casos de meningitis por probióticos. Las pruebas genómicas para identificar genes de resistencia a antibióticos en cepas comerciales puede ser una herramienta valiosa para decidir el uso en cierto tipo de pacientes.
Conclusión.
La evidencia respalda que la microbiota intestinal y la dieta influyen profundamente en la salud mental a través de mecanismos moleculares, inmunológicos y neuronales complejos (Mosquera et al., 2024). Se recomienda a los clínicos:
- Evaluar el estado nutricional y los hábitos dietéticos como parte integral del diagnóstico psiquiátrico.
- Considerar el uso de psicobióticos como terapia adyuvante en trastornos del estado de ánimo, siempre basándose en la evidencia de cepas específicas.
- Fomentar dietas ricas en fibra, polifenoles y ácidos grasos Omega-3 para promover un microbioma saludable y reducir la inflamación sistémica.
- Mantenerse actualizados sobre las investigaciones en curso respecto al eje intestino-cerebro, reconociendo a la comida no solo como energía, sino como un modulador potencial del estado de ánimo y la función neurológica.
Dr. Andrés Naranjo Cuéllar.
Médico y Cirujano.
MSc en Nutrición.

Bibliografía.
Akkasheh, G., Kashani-Poor, Z., Tajabadi-Ebrahimi, M., Jafari, P., Akbari, H., Taghizadeh, M., Memarzadeh, M. R., Asemi, Z., & Esmaillzadeh, A. (2016). Clinical and metabolic response to probiotic administration in patients with major depressive disorder: A randomized, double-blind, placebo-controlled trial. Nutrition, 32(3), 315–320. https://doi.org/10.1016/j.nut.2015.09.003
Allen, A. P., Hutch, W., Borre, Y. E., Kennedy, P. J., Temko, A., Boylan, G., Murphy, E., Cryan, J. F., Dinan, T. G., & Clarke, G. (2016). Bifidobacterium longum 1714 as a translational psychobiotic: Modulation of stress, electrophysiology and neurocognition in healthy volunteers. Translational Psychiatry, 6(11), e939–e939. https://doi.org/10.1038/tp.2016.191
Chicharro, C. (2023, diciembre 4). Triptófano y sus metabolitos. FOM. https://ortegaygasset.edu/triptofano-y-sus-metabolitos/
Dinan, T. G., Stanton, C., & Cryan, J. F. (2013). Psychobiotics: A novel class of psychotropic. Biological Psychiatry, 74(10), 720–726. https://doi.org/10.1016/j.biopsych.2013.05.001
Eskandarzadeh, S., Effatpanah, M., Khosravi-Darani, K., Askari, R., Hosseini, A. F., Reisian, M., & Jazayeri, S. (2021). Efficacy of a multispecies probiotic as adjunctive therapy in generalized anxiety disorder: A double blind, randomized, placebo-controlled trial. Nutritional Neuroscience, 24(2), 102–108. https://doi.org/10.1080/1028415X.2019.1598669
Eslami Shahrbabaki, M., Sabouri, S., Sabahi, A., Barfeh, D., Divsalar, P., Esmailzadeh, M., & Ahmadi, A. (2020). The Efficacy of Probiotics for Treatment of Bipolar Disorder-Type 1: A Randomized, Double-Blind, Placebo Controlled Trial. Iranian Journal of Psychiatry, 15(1), 10–16.
Ghaderi, A., Banafshe, H. R., Mirhosseini, N., Moradi, M., Karimi, M.-A., Mehrzad, F., Bahmani, F., & Asemi, Z. (2019). Clinical and metabolic response to vitamin D plus probiotic in schizophrenia patients. BMC Psychiatry, 19(1), 77. https://doi.org/10.1186/s12888-019-2059-x
Hefnawy, M. (2024). The impact of Gut Microbiota on Mental Health. En Nutrition and Psychiatric Disorders (1 Ed). Springer. https://doi.org/10.1007/978-981-97-2681-3
Jarosz, Ł. S., Socała, K., Michalak, K., Wiater, A., Ciszewski, A., Majewska, M., Marek, A., Grądzki, Z., & Wlaź, P. (2024). The effect of psychoactive bacteria, Bifidobacterium longum Rosell®-175 and Lactobacillus rhamnosus JB-1, on brain proteome profiles in mice. Psychopharmacology, 241(5), 925–945. https://doi.org/10.1007/s00213-023-06519-z
Kazemi, A., Noorbala, A. A., Azam, K., Eskandari, M. H., & Djafarian, K. (2019). Effect of probiotic and prebiotic vs placebo on psychological outcomes in patients with major depressive disorder: A randomized clinical trial. Clinical Nutrition, 38(2), 522–528. https://doi.org/10.1016/j.clnu.2018.04.010
Kim, C.-S., Cha, L., Sim, M., Jung, S., Chun, W. Y., Baik, H. W., & Shin, D.-M. (2021). Probiotic Supplementation Improves Cognitive Function and Mood with Changes in Gut Microbiota in Community-Dwelling Older Adults: A Randomized, Double-Blind, Placebo-Controlled, Multicenter Trial. The Journals of Gerontology. Series A, Biological Sciences and Medical Sciences, 76(1), 32–40. https://doi.org/10.1093/gerona/glaa090
Lee, H., Park, J.-Y., Choi, S.-I., Kim, B.-K., & Lee, J. Y. (2026). Lactobacillus gasseri MG4247 and Lacticaseibacillus rhamnosus MG4644 alleviate LPS-induced cognitive impairment via activation of the Akt/CREB/BDNF signaling pathway. Behavioural Brain Research, 499, 115961. https://doi.org/10.1016/j.bbr.2025.115961
McGuinness, A. J., Davis, J. A., Dawson, S. L., Loughman, A., Collier, F., O’Hely, M., Simpson, C. A., Green, J., Marx, W., Hair, C., Guest, G., Mohebbi, M., Berk, M., Stupart, D., Watters, D., & Jacka, F. N. (2022). A systematic review of gut microbiota composition in observational studies of major depressive disorder, bipolar disorder and schizophrenia. Molecular Psychiatry, 27(4), 1920–1935. https://doi.org/10.1038/s41380-022-01456-3
Moore, Keith. (1985). Anatomía con orientación clínica (2 Ed) [1360]. Panamericana. (Obra original publicada en 1985)
Mosquera, F. E. C., Lizcano Martinez, S., & Liscano, Y. (2024). Effectiveness of Psychobiotics in the Treatment of Psychiatric and Cognitive Disorders: A Systematic Review of Randomized Clinical Trials. Nutrients, 16(9), 1352. https://doi.org/10.3390/nu16091352
Nikolova, V. L., Smith, M. R. B., Hall, L. J., Cleare, A. J., Stone, J. M., & Young, A. H. (2021). Perturbations in Gut Microbiota Composition in Psychiatric Disorders: A Review and Meta-analysis. JAMA Psychiatry, 78(12), 1343–1354. https://doi.org/10.1001/jamapsychiatry.2021.2573
Nutrition and Psychiatric Disorders. An Evidence-Based Approach to Understanding the Diet-Brain connection (1a ed.). (2024). Springer. https://doi.org/10.1007/978-981-97-2681-3 (Obra original publicada en Wael Mohamed and Kobeissy Firas)
Shaaban, S. Y., El Gendy, Y. G., Mehanna, N. S., El-Senousy, W. M., El-Feki, H. S. A., Saad, K., & El-Asheer, O. M. (2018). The role of probiotics in children with autism spectrum disorder: A prospective, open-label study. Nutritional Neuroscience, 21(9), 676–681. https://doi.org/10.1080/1028415X.2017.1347746
Wallace, C. J. K., & Milev, R. V. (2021). The Efficacy, Safety, and Tolerability of Probiotics on Depression: Clinical Results From an Open-Label Pilot Study. Frontiers in Psychiatry, 12, 618279. https://doi.org/10.3389/fpsyt.2021.618279
Wang, L.-J., Yang, C.-Y., Kuo, H.-C., Chou, W.-J., Tsai, C.-S., & Lee, S.-Y. (2022). Effect of Bifidobacterium bifidum on Clinical Characteristics and Gut Microbiota in Attention-Deficit/Hyperactivity Disorder. Journal of Personalized Medicine, 12(2), 227. https://doi.org/10.3390/jpm12020227
Yang, L., Guo, T., Wei, Y., Zhang, Z., Sun, Y., Yan, N., Ding, S., Jiang, L., & Liu, H. (2026). Lactobacillus acidophilus exerts neuroprotective effects in MPTP mice: Potential links to the gut microbiota and GLP-1. Physiology & Behavior, 307, 115229. https://doi.org/10.1016/j.physbeh.2026.115229
Yuan, N., Chen, Y., Xia, Y., Dai, J., & Liu, C. (2019). Inflammation-related biomarkers in major psychiatric disorders: A cross-disorder assessment of reproducibility and specificity in 43 meta-analyses. Translational Psychiatry, 9(1), 233. https://doi.org/10.1038/s41398-019-0570-y