¿Qué es la mitocondria y para qué sirve?
La mitocondria es el organelo celular encargado de generar energía, interfiere en el metabolismo de carbohidratos, proteínas y lípidos. La mitocondria está especializada en funciones como la β–Oxidación, el ciclo de la urea, metabolismo de aminoácidos y esteroides y lo más importante en el ciclo del ácido tricarboxilico o ciclo de Krebs.
¿Cómo se formó la mitocondria?
Los biólogos evolucionistas consideran la que la “teoría endosimbiótica” es la más probable en cuanto a la formación de las mitocondrias y en general de la formación de las células eucariotas.
Esta teoría endosimbiótica plantea, que las células eucariotas se desarrollaron a partir de dos células procariotas que se juntaron en una relación simbiótica: una arquea y por el otro lado una bacteria. La arquea brindó protección y alimento, mientras que la bacteria (que eventualmente se convirtió en la mitocondria) aportó la capacidad de detoxificación del oxígeno, con la capacidad de convertir el oxígeno en gas carbónico y agua, con la ventaja de proporcionar energía en este proceso.
De hecho, existen muchas similitudes entre la mitocondria actual y sus predecesores las bacterias. El más obvio es la morfología, la mitocondria mide 1 µm, que es el tamaño de la mayoría de las bacterias; también se parecen en qué, tanto la mitocondria como las bacterias tienen doble membrana y en el hecho de que su DNA sea circular.
Genoma mitocondrial.
El genoma mitocondrial está organizado de forma circular, tiene dos cadenas una pesada externa y otra ligera interna, tiene 16.569 pares de bases (pb) que codifican 37 genes, y al igual que el DNA bacteriano, carece de intrones.
De estos 37 genes, 13 codifican para polipéptidos que están involucrados en la respiración mitocondrial (fosforilación oxidativa); 22 codifican para RNA de transferencia (tRNAs), los cuales están estratégicamente ubicados en el genoma, para que la traducción de esos 13 polipéptidos se realice fácilmente; y 2 que codifican para RNA ribosomal (rRNAs), las subunidades 12s y 16s.
Diferencias entre el DNA mitocondrial (mtDNA) y el DNA nuclear (nDNA).
Existen varias diferencias entre el DNA mitocondrial (mtDNA) y el DNA nuclear (nDNA):
- El mtDNA tiene una herencia materna. Las mitocondrias del espermatozoide no entran al ovulo, una madre que tenga una mutación mitocondrial la pude transmitir a su hijo varón, pero solo las hijas la transmitirán a sus descendientes.
- Heteroplasmicidad. En una sola célula hay miles de mitocondrias, las mutaciones mitocondriales normalmente afectan a algunas mitocondrias y no a todas, a esto se le llama heteroplasmicidad. Dependiendo de la proporción de mitocondrias afectadas, se desarrolla un determinado fenotipo, a este concepto se le llama el umbral de expresión.
- Segregación mitótica. No todas las células ni todos los tejidos se afectan en la misma medida; Así los órganos que dependen más de la respiración aeróbica, y cuyas células tienen más mitocondrias (músculo y cerebro), se encuentran más afectados en los casos de alguna mutación.
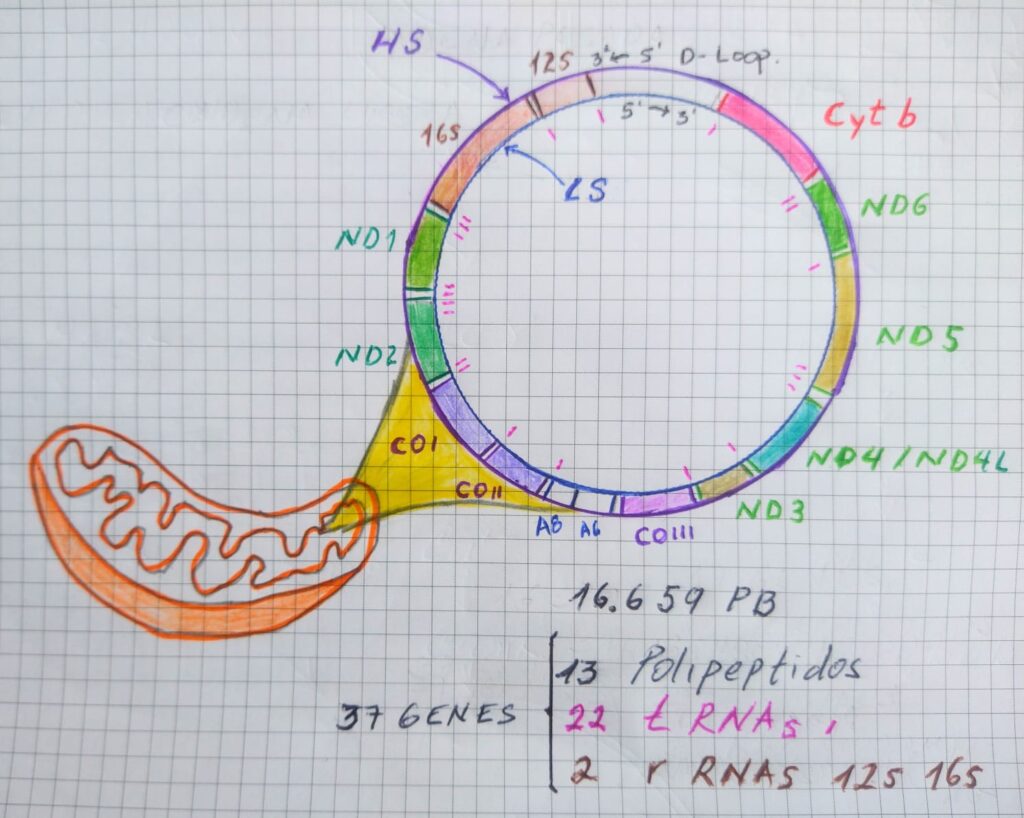
Esquema representativo del DNA mitocondrial (mtDNA), compuesto de 16.659 parres de bases (pb), que codifican 37 genes. El mtDNA carece de intrones. De los 37 genes; 13 codifican para polipéptidos relacionada con funciones para la cadena respiratoria, 22 codifican para RNA de transferencia (tRNAs) y 2 para RNA ribosomal (rRNAs). 12s, gen que codifica subunidad rRNA 12s de mitoribosomas; 16s, gen que codifica la subunidad rRNA 16s de mitoribosomas; A6, subunidad A6 de ATP sintasa; A8, subunidad A8 de ATP sintasa; Cyt b, Citocromo b; CO, Citocromo c oxidasa; D-Loop, Promotores para transcripción de mtDNA; LS, cadena liviana; HS, cadena pesada; ND, subunidades de NADH-coenzima Q oxidorreductasa. Fuente: Elaboración propia.
Cadena respiratoria – Fosforilación Oxidativa.
La principal función de la mitocondria es generar energía a partir de oxígeno, para esto se vale de dos transportadores de hidrógeno, NADH y FADH2, y una serie de complejos proteicos (complejos I al IV, algunos de ellos con citocromos que son moléculas con grupos hemo en su estructura).
- Complejo I: NADH-Q Oxidorreductasa (NADH deshidrogenasa).
- Complejo II: Coenzima Q + (succinato/ubiquinona oxidorreductasa o succinato deshidrogenasa).
- Complejo III: Q citocromo c oxidorreductasa (Complejo bc1).
- Complejo IV: citocromo c oxidasa.
- Complejo V: ATP sintasa.
Los transportadores de hidrógeno NADH y FADH2 junto con los complejos proteicos reducen el O2 a H2O y permiten crear un gradiente de protones entre el espacio mitocondrial y la matriz mitocondrial.
Este gradiente de protones es aprovechado por la ATPasa sintasa (complejo V), para utilizar el retorno del H+ desde el espacio intermembrana a la matriz, como fuente para la generación de energía utilizando ADP para formar ATP.
En otras palabras, para lograr oxidar el oxígeno a H2O, y a la vez generar energía en forma de ATP, la mitocondria se vale de los cuatro complejos proteicos (I al IV), qué se encargan de transferir electrones desde NADH y FADH2 al oxígeno y crear un gradiente de protones; y de un complejo proteico ATP sintasa (también llamado complejo V) que funciona como generador de energía, y qué utiliza el gradiente de H+ que los otros complejos I al IV crearon.
Proceso fisiológico de la cadena respiratoria o Fosforilación Oxidativa:

Representación esquemática de la cadena respiratoria o fosforilación oxidativa.
La transferencia de electrones del Complejo I al Complejo III está mediada por el Complejo II; y la transferencia del Complejo III al Complejo IV está mediada por la pequeña proteína citocromo c (CytC).
El O2 también se reduce por los electrones que provienen de FADH2 en el Complejo II, (succinato / ubiquinona oxidorreductasa, la acil-CoA deshidrogenasa y glicerol-fosfato deshidrogenasa, representadas con un rectángulo violeta). Los electrones de FADH2 se transfieren a ubiquinona y luego fluyen al O2 a través del Complejo III y complejo IV, como sucede con el NADH.
ATP, adenosín trifosfato; CO, Citocromo c oxidasa; CoQ, Coenzima Q o ubiquinona; Cytb, Citocromo b; CytC, Citocromo C; e–, electrones; EIM, espacio intermembrana; FADH, Flavin Adenin Dinucleótido Reducido; H+, ion hidrógeno; MME, membrana mitocondrial externa; MMI, membrana mitocondrial interna; NADH, Nicotin Adenin Dinucleótido Reducido. Fuente: Elaboración propia.
Manifestaciones clínicas de las mutaciones en el genoma mitocondrial.
En el mtDNA está ubicado en casi todas las células del organismo, lo cuál explica el hecho de que las mtDNA puede dar síntomas en casi todos los tejidos del cuerpo. Además, como se mencionó anteriormente, la heteroplasmicidad (el hecho de que la mutación puede estar presentes en algunos mtDNA y en otros no), hace que la gravedad de las manifestaciones varíe dependiendo de qué proporción de mtDNA mutado está presente (umbral de expresión).
Hay cuatro fenotipos clásicamente descritos en las mutaciones de mtDNA:
MELAS (Mitochondrial encephaomyopathy, lactic acidosis, and stroke-like episodies).
Las manifestaciones clínicas empiezan después de los 40 años, se caracteriza por encefalopatía con episodios convulsivos, demencia temprana, los síntomas más comunes son: intolerancia al ejercicio, sordera, ptosis palpebral, migraña y alteraciones gastrointestinales.
MELAS está más frecuentemente asociado con la mutación 3243A>G en el gen (MTTL) y con m. 13513G>A en el gen (MTND5).
MERF (Myoclonic epilepsy with ragged-red fibers).
Es un síndrome multisistémico caracterizado por mioclonía, epilepsia y debilidad, pérdida de la audición, ptosis y múltiples lipomas, con hallazgos característicos en la biopsia de músculo, que cada vez es menos frecuente, pues ha sido remplazado por la secuenciación completa del genoma mitocondrial.
Hasta ahora la m.8344A>G en el gen (MTTK) se ha relacionado con este síndrome.
NARP (Neuropathy, ataxia, retinitis pigmentosa) y MILS (Maternally inheretid Leigh síndrome).
Usualmente afecta personas jóvenes y se caracteriza por demencia, convulsiones, ataxia, debilidad proximal y neuropatía sensora. Dentro de este síndrome se puede incluir el síndrome de MILS (Maternally inheretid Leigh síndrome), en ambos casos la mutación ocurre en el gen MT-ATP6, la diferencia en la severidad es que mientras el NARP afecta cerca del 70% del genoma mitocondrial, en el MILS afecta a un 90%.
LHON (Leber hereditary optic neropathy).
Se caracteriza por perdida indolora, subaguda de la visión central asociada a discromatopsia (disminución de la percepción del color) en personas jóvenes y se presenta más frecuentemente en el sexo masculino.
Las mutaciones del Complejo I están asociadas a este síndrome, y se ha asociado con m.11779G>A in MTND4; m.3460G>A en MTND1; y m.14484T>C en MTND6.
Patologías frecuentes en la atención primaria, también se han relacionado con mutaciones en mtDNA.
Síndrome de Fatiga Crónica (SFC).

En un estudio multicéntrico, multidisciplinario realizado por investigadores de Estados Unidos y Canadá, publicado el pasado 21 de septiembre en la revista Medical Hypotheses, los investigadores plantean que una enfermedad muy común, el Síndrome de Fatiga Crónica (SFC) es causado por una insuficiencia metabólica mitocondrial inducida por factores de estrés, que dan como resultado una disminución los metabolismos anabólicos suficientes para producción de energía por parte de la célula.
Tratamiento de las enfermedades mitocondriales.
Al momento de escribir este artículo, las enfermedades del mtDNA solo tienen tratamiento sintomático y de soporte de terapias respiratoria, física, pero no ha sido aprobado ningún tratamiento curativo.
La dieta forma parte fundamental, ya que disminuye los productos nocivos que pueden incrementar los síntomas, el ejercicio aeróbico también es parte importante del tratamiento.
La terapia de liberación de genes en la mitocondria, a pesar de ser una medida controversial, ha tenido buenos resultados en los estudios preclínicos en pacientes con Síndrome LHON.
Debido a que hasta el momento los experimentos genéticos con células germinales están restringidos, no se han podido extender el beneficio de una posible terapia de prevención de mutaciones mtDNA a través de técnicas de donación mitocondrial (el ovocito tendría nDNA de su madre biológica, pero mtDNA de un donador).
El único compuesto bioactivo con el que contamos en la medicina funcional que tiene estudios científicos que avalan su uso en enfermedades mitocondriales es la Coenzima-Q (ubiquinona).

Dr. Andrés Naranjo Cuéllar
Médico y Cirujano.
MsC en Nutrición.

Bibliografía
Harper Bioquímica Ilustrada (2018), 31 Ed. McGraw-Hill.
Integrative Human Biochemistry (2015) Ed Springer.
Rosemberg´s Molecular and Genetic Basis of Neurological and Psychiatric Diseases. (2021) 6 Ed. Elsevier.
https://pubmed.ncbi.nlm.nih.gov/34358921/






